Spondylodiscite : infection vertébro-discale, diagnostic et traitement
La spondylodiscite est une infection rare mais potentiellement grave qui touche simultanément un disque intervertébral et les deux corps vertébraux adjacents. Son nom évoque sa double topographie : « spondylo- » pour les vertèbres et « discite » pour le disque intervertébral. Cette infection ostéo-articulaire profonde reste un défi diagnostique majeur car ses symptômes — douleurs dorso-lombaires intenses, parfois sans fièvre — sont peu spécifiques et facilement attribués à tort à un simple « mal de dos ».
Son incidence en France est estimée à 2,4 cas pour 100 000 habitants par an, et augmente avec le vieillissement de la population, le développement de la chirurgie rachidienne, l’augmentation des terrains immunodéprimés (chimiothérapies, biothérapies, diabète) et le recours croissant à des dispositifs vasculaires invasifs.
Comprendre la spondylodiscite, c’est savoir reconnaître à temps une urgence diagnostique souvent négligée — un retard de prise en charge expose à des complications neurologiques irréversibles (compression médullaire, paraplégie) et à une mortalité qui reste comprise entre 2 et 11 % malgré les progrès thérapeutiques.
À retenir
- La spondylodiscite est une infection rare mais grave touchant simultanément un disque intervertébral et les deux vertèbres adjacentes.
- Elle représente 2 à 7 % des infections ostéo-articulaires, avec une incidence en augmentation (vieillissement, immunosuppression).
- Le diagnostic est souvent retardé de 2 à 6 mois : douleurs dorso-lombaires intenses, persistantes, nocturnes, parfois sans fièvre.
- Le germe le plus fréquent est le staphylocoque doré (50 % des cas), suivi des bacilles à Gram négatif et de la tuberculose.
- Le traitement repose sur une antibiothérapie intraveineuse prolongée (6 à 12 semaines) et un repos rachidien.
Anatomie et physiopathologie
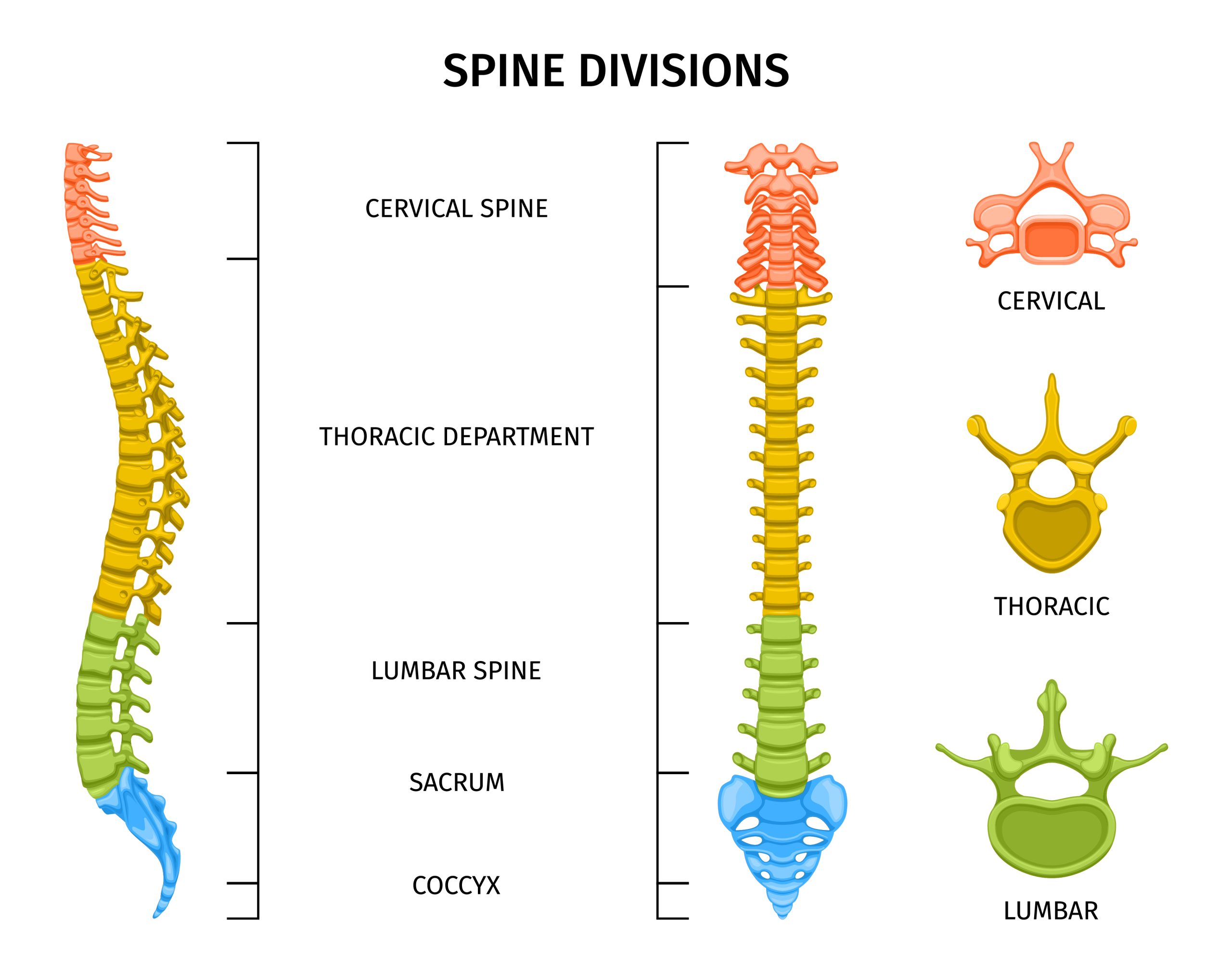
La colonne vertébrale est composée de 33 vertèbres séparées par des disques intervertébraux fibrocartilagineux, structures peu vascularisées qui amortissent les pressions axiales. Chez l’adulte, le disque est avasculaire en son centre, ce qui le rend particulièrement vulnérable aux infections : une fois le germe implanté, les défenses immunitaires y parviennent difficilement.
L’infection débute généralement dans la partie sous-chondrale de la vertèbre, près du plateau vertébral richement vascularisé. Elle s’étend ensuite au disque adjacent puis à la vertèbre voisine, formant un foyer infectieux centré sur l’espace inter-vertébral. À mesure que l’infection progresse, elle peut s’étendre aux tissus mous environnants (formation d’abcès paravertébraux, épidurite, abcès psoas), et plus rarement comprimer la moelle ou les racines nerveuses.
Trois grandes voies de contamination
Voie hématogène (la plus fréquente, 60 à 80 % des cas). Le germe atteint le rachis par voie sanguine depuis un foyer primaire à distance : infection cutanée, urinaire, dentaire, endocardite, cathéter veineux infecté. C’est la voie classique des spondylodiscites à staphylocoque doré.
Voie iatrogène (post-chirurgicale). Survenue dans les semaines ou mois suivant une chirurgie du rachis (laminectomie, arthrodèse, prothèse discale) ou une infiltration épidurale. Représente 10 à 30 % des cas selon les séries, en augmentation avec le développement de la chirurgie rachidienne.
Voie contiguë (rare). Extension d’une infection des tissus mous voisins : abcès psoas, infection viscérale rétropéritonéale, plaie pénétrante.
Les germes en cause
Staphylococcus aureus (staphylocoque doré) est de loin le germe le plus fréquent (40 à 50 % des cas) [4]. Sa prévalence augmente avec la dissémination des staphylocoques dorés résistants à la méticilline (SARM), nosocomiaux ou communautaires.
Bacilles à Gram négatif (E. coli, Klebsiella, Proteus, Pseudomonas) : 15 à 30 % des cas. Souvent secondaires à une infection urinaire négligée, en particulier chez le sujet âgé diabétique. Pseudomonas aeruginosa est fréquent chez les toxicomanes intraveineux.
Streptocoques (notamment Streptococcus agalactiae chez l’âgé, Streptococcus mutans en cas de foyer dentaire) : 5 à 15 %.
Mycobacterium tuberculosis (mal de Pott) : la tuberculose vertébrale reste fréquente dans les pays à forte endémie tuberculeuse et chez les migrants. Évolution plus indolente, atteinte préférentielle du rachis thoracique, abcès paravertébraux fréquents avec extension psoatique.
Brucella spp. (brucellose) : à évoquer en contexte épidémiologique évocateur (consommation de lait cru, contact avec ruminants, séjour en zone d’endémie).
Candida spp. et champignons : très rares, principalement chez l’immunodéprimé profond ou en post-chirurgie.
Symptômes
La présentation clinique est trompeuse, ce qui explique le retard diagnostique fréquent (médiane : 2 à 4 mois entre les premiers symptômes et le diagnostic) [4].
Douleurs rachidiennes : symptôme cardinal, présent chez plus de 85 % des patients. Douleur localisée précisément en regard du foyer infectieux, augmentée par les mouvements et la mise en charge, et — c’est un signe d’alarme essentiel — présente la nuit, réveillant le patient (contrairement aux douleurs mécaniques classiques qui se calment au repos). La raideur du segment atteint est constante.
Fièvre : présente chez seulement 50 à 60 % des patients, souvent modérée (38-38,5 °C), parfois intermittente, parfois absente — surtout chez le sujet âgé et l’immunodéprimé. L’absence de fièvre ne doit JAMAIS faire éliminer le diagnostic.
Altération de l’état général : asthénie, amaigrissement, anorexie, plus marqués dans les formes tuberculeuses et brucelliennes.
Signes neurologiques : présents dans 15 à 30 % des cas et imposent une prise en charge urgente. Sciatique ou cruralgie en cas d’atteinte lombaire, syndrome pyramidal en cas d’atteinte cervico-dorsale, troubles sphinctériens, paraplégie progressive dans les formes négligées avec compression médullaire (urgence neurochirurgicale absolue).
À propos de l’auteur
Docteur en biochimie, Marc Fontaine est rédacteur scientifique pour Science & Santé. Il consacre sa pratique à la vulgarisation rigoureuse des connaissances médicales, en s’appuyant exclusivement sur des études cliniques publiées dans des revues à comité de lecture.
Diagnostic biologique
Le bilan biologique apporte des arguments mais ne permet jamais à lui seul le diagnostic.
Syndrome inflammatoire : CPK habituellement normale, mais CRP élevée (présente dans 95 % des cas), VS accélérée, hyperleucocytose modérée (inconstante). La CRP est l’élément le plus utile pour le suivi du traitement.
Hémocultures : positives dans 50 à 70 % des cas, surtout si elles sont prélevées en période fébrile. Indispensables avant toute antibiothérapie.
Bandelette urinaire et ECBU systématiques (recherche de la porte d’entrée urinaire).
Sérologies ciblées selon le contexte : brucellose, syphilis, VIH, hépatites.
Bilan de la porte d’entrée : examen cutané, dentaire, recherche d’endocardite (échographie cardiaque transœsophagienne), bilan urinaire.
Imagerie : place centrale dans le diagnostic
L’imagerie est essentielle au diagnostic et à la surveillance.
Radiographies standard du rachis : retardées (signes radiographiques apparaissant après 2 à 4 semaines d’évolution). Pincement de l’interligne discal, érosion des plateaux vertébraux adjacents, parfois géode, tassement vertébral. Peu sensibles dans les formes précoces.
IRM du rachis (examen de référence) : sensibilité et spécificité > 90 % dès la première semaine. Hypersignal T2 et hyposignal T1 du disque et des plateaux adjacents, prise de contraste après injection de gadolinium, visualisation des abcès paravertébraux et épiduraux. À demander en urgence devant toute suspicion clinique [5].
Scanner du rachis : alternative à l’IRM si celle-ci est contre-indiquée (pacemaker, claustrophobie). Permet aussi de guider une biopsie discale percutanée.
TEP-scanner au FDG : utile dans les formes atypiques ou pour le suivi évolutif.
Documentation microbiologique : indispensable
La documentation du germe en cause est cruciale pour adapter l’antibiothérapie. Elle repose sur :
Hémocultures : à prélever systématiquement, idéalement en période fébrile, avant toute antibiothérapie.
Biopsie discale percutanée scanno-guidée : examen de référence en l’absence de positivation des hémocultures. Réalisée en radiologie interventionnelle sous anesthésie locale, elle prélève quelques fragments de disque et de tissu inflammatoire pour examen bactériologique, mycologique, mycobactériologique et anatomopathologique. Rentabilité : 50 à 70 % si elle est réalisée avant toute antibiothérapie.
Biopsie chirurgicale : indiquée en cas d’échec de la biopsie percutanée ou en cas de complication chirurgicale (abcès volumineux, compression médullaire).
En l’absence de documentation microbiologique, une antibiothérapie probabiliste à large spectre couvrant le staphylocoque doré et les bacilles Gram négatifs est instaurée.
Traitement
Le traitement repose sur trois piliers : antibiothérapie prolongée, immobilisation, et chirurgie en cas de complication.
Antibiothérapie : adaptée au germe isolé. Durée totale historiquement de 12 semaines, ramenée à 6 semaines dans les spondylodiscites non compliquées par un essai randomisé majeur (Bernard et al., Lancet 2015, qui a démontré la non-infériorité d’un traitement court) [6]. Les molécules les plus utilisées : oxacilline, cloxacilline, céfazoline (staphylocoques sensibles à la méticilline), vancomycine ou daptomycine (staphylocoques résistants), céphalosporines de 3e génération, fluoroquinolones, rifampicine (en association). Voie intraveineuse pendant 2 à 4 semaines puis relais oral. Pour la tuberculose : quadrithérapie classique pendant 9 à 12 mois.
Immobilisation rachidienne : repos strict au lit initialement, puis port d’un corset rigide pendant 6 à 12 semaines pour soulager les douleurs et prévenir les complications mécaniques (tassement vertébral, cyphose).
Chirurgie : indiquée en cas de compression médullaire ou radiculaire avec déficit neurologique, abcès volumineux non drainable percutanément, instabilité rachidienne, déformation progressive, échec du traitement médical bien conduit. Décompression, drainage des abcès, parfois arthrodèse rachidienne.
Antalgie adaptée à la douleur (souvent intense : paliers 2 voire 3).
Suivi : clinique (douleur, neurologie), biologique (CRP normalisée en 4-6 semaines), radiologique (IRM à 3 et 6 mois).
Pronostic et complications
Le pronostic dépend du germe en cause, du délai de prise en charge, de l’âge et des comorbidités du patient.
Mortalité globale : 2 à 11 % selon les séries, plus élevée chez le sujet âgé, l’immunodéprimé et en cas de retard diagnostique.
Complications neurologiques : 15 à 30 % des patients à la phase aiguë (radiculalgie, syndrome de la queue de cheval, paraplégie). Récupération souvent incomplète si la prise en charge est retardée.
Séquelles mécaniques : tassement vertébral, cyphose, instabilité, douleurs chroniques résiduelles dans 30 à 60 % des cas.
Récidive : rare (< 5 %) si l'antibiothérapie est bien menée et la porte d'entrée traitée.
Prévention
La prévention repose sur la maîtrise des facteurs de risque : traitement précoce des infections urinaires, cutanées et dentaires (notamment chez les diabétiques et immunodéprimés), asepsie rigoureuse lors des gestes invasifs rachidiens et péri-rachidiens, équilibre du diabète, limitation des antibiothérapies inutiles favorisant les résistances, prise en charge attentive des cathéters veineux centraux.
Quand consulter
Plusieurs situations imposent une consultation rapide : douleurs dorso-lombaires intenses et persistantes depuis plus de 2 semaines, surtout si elles sont nocturnes ou si elles réveillent ; association à une fièvre, même modérée ; antécédent récent d’infection bactérienne, de chirurgie rachidienne ou d’infiltration épidurale ; sujet à risque (diabète, immunosuppression, toxicomanie, cathéter central) ; survenue de signes neurologiques (faiblesse des membres, troubles sphinctériens, sciatique récente sans cause mécanique évidente). Devant des signes neurologiques aigus, l’appel au 15 (SAMU) est justifié.
Conclusion
La spondylodiscite est l’archétype de la pathologie rare mais grave dont le diagnostic doit être systématiquement évoqué devant des douleurs rachidiennes persistantes et atypiques. Le diagnostic précoce, par l’IRM rachidienne, et la documentation microbiologique par hémocultures et biopsie discale, conditionnent un pronostic favorable. L’antibiothérapie prolongée et l’immobilisation rachidienne permettent une guérison dans la grande majorité des cas. La principale erreur à éviter est l’instauration d’une antibiothérapie probabiliste avant toute documentation microbiologique : elle compromet définitivement l’identification du germe et le traitement adapté qui en découle.
Sources scientifiques
- Berbari EF, et al. 2015 Infectious Diseases Society of America (IDSA) Clinical Practice Guidelines for the Diagnosis and Treatment of Native Vertebral Osteomyelitis in Adults. Clinical Infectious Diseases, 2015. Oxford Academic — CID
- Zimmerli W. Vertebral osteomyelitis. The New England Journal of Medicine, 2010. NEJM
- Société de Pathologie Infectieuse de Langue Française. Spondylodiscites infectieuses primitives — recommandations. Médecine et Maladies Infectieuses, 2007. SPILF
- Mylona E, et al. Pyogenic vertebral osteomyelitis: a systematic review of clinical characteristics. Seminars in Arthritis and Rheumatism, 2009. ScienceDirect
- HAS. Imagerie de la spondylodiscite — recommandations de bonne pratique. Haute Autorité de Santé. HAS
- Bernard L, et al. Antibiotic treatment for 6 weeks versus 12 weeks in patients with pyogenic vertebral osteomyelitis: an open-label, non-inferiority, randomised, controlled trial. The Lancet, 2015. The Lancet